[뉴스비전e 김혜진 기자] 최근 의료 시장이 기존 질병치료 중심에서 개인 건강관리 및 예방으로 변화되면서 암 등 불치병을 정복할 수 있는 유전자 치료에 대한 관심이 증폭되고 있다.
유전자 치료란 유전자 발현체계(gene expression system)를 이용해 치료 유전자를 질병 부위에 전달하고 이상 유전자를 대치하거나 그 부위에 치료용 단백질을 생산케 하여 질병을 치료하는 새로운 치료법을 말한다.
쉽게 말하면, 치료용 유전자를 생체 내에 적절히 발현시켜 병을 치료하는 방법이다.
최초의 유전자치료제인 글리베라의 유럽판매 승인 이후 전세계 국가들은 부작용이 거의 없고 가격이 비싸 고부가가치 상품인 유전자 치료제 개발에 앞다퉈 나서고 있다.
첨예한 화두로 부각되고 있는 꿈의 차세대 의약품 유전자 치료제에 대해 연재를 통해 집중 분석한다. [편집자 주]
[① "결핍·결함 유전자 교체...질병의 근본을 치료한다"]
유전자 치료제는 결핍이나 결함이 있는 유전자를 교정 · 교체시켜 질병의 근본적인 문제를 치료하는 치료제를 의미한다.
현재 유전자 치료제의 접근방법은 정상기능 유전자를 게놈 안에 삽입해 비정상 기능 유전자를 대체하는 방법, 상동재조합(Homologous Recombination)을 통해 결함 유전자를 정상 유전자로 교체하는 방법, 선택적 역 돌연변이(Selective Reverse Mutation)를 통해 결함 유전자를 정상 기능으로 교정하는 방법 등이 있다.
유전자 치료제의 경우 치료용 유전자와 유전자 전달체로 구성되며, 전달체의 경우 아데노바이러스, AAV(Adeno-Associate Virus)와 같은 바이러스성 전달체와 리포좀, Naked DNA와 같은 비 바이러스성 전달체로 구분된다.
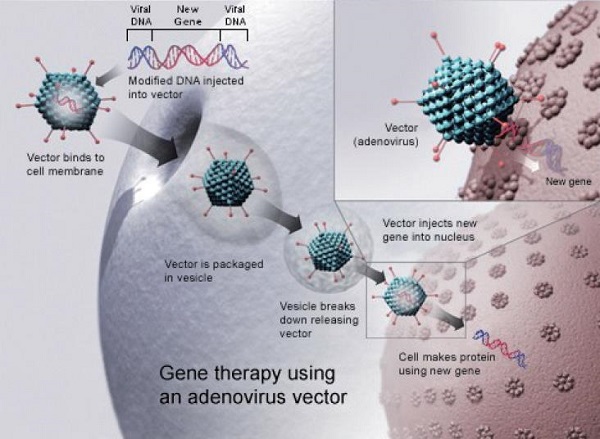
유전자 치료제의 경우, 최초의 임상실험이 1990년에 시작됐으며, 2003년 중국의 쉔젠 시바이오노 진테크의 '젠디신(Genedicine)'이 중국에서 제품허가를 받은 것이 최초의 유전자 치료제 허가 사례이다.
유럽, 미국 등 비교적 큰 의약품 시장 규모를 가지는 지역에서의 허가는 최근에 이르러서야 이뤄지게 됐는데, 2012년 지단백 지질분해 효소결핍증(LDLP) 치료제인 '글리베라(Glybera)'가 유럽에서 승인을 받았고, 항암 유전자 치료제인 '임리직(Imlygic)'이 2015년에 미국 허가를 받았다.
가장 최근에 허가된 유전자 치료제는 스위스계 제약사인 노바티스가 만든 백혈병 유전자 치료제 ‘킴리아(Kymriah)’로, 지난 8월 30일 미국 식품의약청(FDA)로부터 승인을 받았다.
우리나라 코오롱생명과학도 지난 7월 국내 최초의 유전자 치료제인 인보사에 대한 판매허가를 받았다.
희귀질환인 중증 복합형 면역결핍증(ADA-SCID) 치료제인 글락소 스미스클라인의 '스트림벨리스(Strimvelis)'는 지난해 6월 유럽 허가를 받았다. 이 치료제는 최초의 생체 외(ex-vivo) 줄기세포 유전자 치료제로 이름을 올렸다.
현재 개발 중인 유전자 치료제가 2012년 이후 약 2배 이상 증가했다는 점에서 유전자 치료제의 본격적인 상용화가 조만간 이뤄질 것으로 전망되고 있다.

